Zulassungsdesaster der Covid "Impfstoffe" bei der Europäischen Union?
- Transparenztest

- 26. Feb. 2023
- 8 Min. Lesezeit
26. Februar 2023
"Das Zulassungsdesaster: Lobbyarbeit und Rechtsbruch im Fall der mRNA- Präparate?"
Die Berliner Zeitung BZ veröffentlichte am 12. Februar 2023 mit diesem Titel einen Artikel von sieben Juristen (RA René M. Kieselmann, Prof. Dr. Gerd Morgenthaler, Dr. Amrei Müller, Prof. Dr. Günter Reiner, RA Dr. Patrick Riebe, RAin Dr. Brigitte Röhrig und Prof. Dr. Martin Schwab).
Das 7-köpfige Juristen-Kollektiv kommt dabei zu einem vernichtenden Ergebnis. Die Zulassung erfolgte nicht Richtlinien konform. Sie verstieß gegen zwingend rechtliche Anforderungen für eine reguläre Zulassung der genbasierten Impfstoffe.
Juristen-Kollektiv: Durch Auflösung der Placebo-kontrollierten Studien waren essentielle Bedingungen nicht erfüllt. Die reguläre Zulassung hätte nach Verordnung 726/2004/EG zwingend abgelehnt werden müssen.
Danach verschwand der Artikel mysteriöser Weise spurlos sowohl auf der Webseite der Berliner Zeitung als auch im BZ Twitter Account. Der Artikel war sogar nicht einmal mit der Google Suchmaschine mehr auffindbar.
Dies war mehr als auffällig. Auch, dass der Artikel per Google Suchmaschine systematisch gelöscht wurde, spricht für eine enge Absprache mit den Internetdiensten. Eine solch systematisch Löschung eines Artikels einer deutschen bekannten Zeitung ohne weitere Hinweise gibt es äußerst selten.
Alternative Medien thematisierten diese befremdliche Vorgehensweise mehrmals hier und hier. Irgendwas merkwürdiges muss sich ereignet haben,
Nach dem darauf folgenden medialen Shitstorm u.a. auf Twitter nahm daraufhin die Berliner Zeitung Stellung. Sie kündigte nach der überraschenden "Depublizierung" eine "Republizierung" des Artikels mit einer gegnerischen Stellungsnahme an. Nach Angaben des Chefredakteurs der BZ war der Grund für die Rücknahme des Artikels, dass man sich mit "starken" Argumenten konfrontiert sah, die die "Richtigkeit" des Textes infrage stellen würde.
Am 16.02.23 wurde der Artikel "republiziert" mit dem neuen Titel:
"Gab es bei den Impfungen ein "Zulassungsdesaster"? Zwei Perspektiven
Die BZ gab als Begründung für ihr merkwürdiges Verhalten folgenden Transparenz Hinweis an:


Merkwürdig hierbei: Ein Molekularbiologe, Emanuel Wyler von der Helmholtz-Gemeinschaft, und nicht ein Jurist oder gar Juristenteam, bezieht Stellung zum Artikel der sieben Juristen.
Die elementaren Kritikbestandteile der Rechtswissenschaftler am Zulassungsverfahren und die inhaltlichen Einwände des Molekularbiologen dem gegenüber sollen im folgenden dargestellt werden.
Juristen-Kollektiv: Reguläre Zulassung ohne Erfüllung der Auflagen
Das Juristen-Kollektiv kommt in seiner Analyse zum Schluss, dass die EU-Kommission im Oktober 2022 die bedingten Zulassungen für Pfizer/Biontech und Moderna in reguläre Zulassungen umgewandelt hat, ohne dass die vorgeschriebenen Auflagen hierzu erfüllt waren.

Die Juristen monieren konkret, dass nach Art 14a Abs. 8 der Verordnung Nr. 726/2004/EG und Art. 7 der Kommissionsverordnung Nr. 507/2006/EG essentielle Zulassungsbedingungen nicht erfüllt wurden. Eine bedingte Zulassung darf aber demnach erst dann in eine reguläre Zulassung umgewandelt werden, wenn der Hersteller alle Bedingungen erfüllt hat.
Art 14a Abs. 4- 8 Verordnung Nr. 726/2004/EG

Durch frühzeitige Auflösung der Kontrollgruppe können die Bedingungen nun nicht mehr erfüllt werden. Eine reguläre Zulassung ist nach den Bestimmungen der Verordnungen folglich nicht mehr zulässig.

Das Juristen-Kollektiv beanstandet hier, dass die Bedingungen der Placebo-kontrollierten Studien nicht erfüllt waren. Ohne solche validen Studien muss jedoch die reguläre Arzneimittelzulassung laut Art. 12 Abs. 1 der Verordnung 726/2004/EG zwingend abgelehnt werden.

Die Kontrollgruppe der Zulassungsstudie wurde mit dem Argument aufgelöst, dass es ethisch problematisch sei, ungeimpfte Personen den Impfstoff für eine gewisse Zeit vorzuenthalten.
Das Juristen-Kollektiv argumentiert dagegen, dass es vielmehr unethisch gewesen ist, ein Präparat weltweit freizugeben, welches nicht systematisch gemäß den Verordnungsbedingungen mittels Kontrollgruppe (Placebo) auf längerfristige Wirksamkeit und Nebenwirkungen evaluiert worden ist.
Vor allem die Sicherheit (Impf Nebenwirkungen) wurde hierdurch nicht ausreichend geprüft.
Dieses Argument wirkt stichhaltig. Denn im ersten Fall wären nur wenige und noch dazu freiwillige Probanden der Kontrollgruppe dem "Risiko" ausgesetzt nicht "geimpft" zu sein. Im Falle eine Erkrankung wären sie dann möglicherweise weniger geschützt als Geimpfte. Im zweiten Falle dagegen lässt man einen neuartigen genbasierten mRNA Impfstoff auf die gesamte Weltbevölkerung los ohne vorher hinsichtlich der Sicherheit bzw. der kurz-, mittel- und langfristigen Nebenwirkungen ausreichend wissenschaftliche Informationen gesammelt zu haben.
Rechtliche Bedingungen sind klar definiert
Die Zulassungsstudie hätte über mehrere Jahre geführt werden müssen. Am Ende war ein finaler Abschlussbericht vorgeschrieben. Durch die frühzeitige Auflösung der Kontrollgruppe wenige Monate nach Start wurde die gesamte Zulassungsstudie jedoch wertlos. Mittel- oder Langfristige Nebenwirkungen können nicht mehr aussagekräftig erhoben werden. Hierdurch macht auch der geplante Abschlussbericht als Zulassungskriterium für die reguläre Zulassung keinen Sinn mehr. Durch Entwertung bzw. Wegfall der ordentlichen Zulassungsstudie mit Kontrollgruppe sowie durch Wegfall des Abschlussberichtes sind jedoch die Bedingungen gemäß der oben genannten Verordnungen nicht mehr erfüllbar.
Prüfung der Sicherheit hinsichtlich Impfnebenwirkungen blieb außen vor
Bei dieser enormen Anzahl an Versuchspersonen (Weltbevölkerung) wird es jedoch aufgrund der Nebeneffekte - die immer zu erwarten sind - zu einer enormen Zahl an Betroffenen mit Impfnebenwirkungen kommen. Das Risiko betrifft hier zudem auch jüngere Altersgruppen, bei denen nur geringe Risiken im Falle einer Erkrankungen zu erwarten sind.
Allein aus diesem Grund sind die Zulassungsstudien mit Doppelblind-Design und Kontrollgruppe obligatorisch vorgeschrieben.
Nach geltenden Recht ist eine reguläre Zulassung ohne Erfüllung der Auflagen nicht vorgesehen. Auf die Bedeutung der Placebo-kontrollierten Studie hat das 7-köpfige Juristen-Kollektiv entsprechend deutlich hingewiesen:
"Beobachtungsdaten aus der milliardenfachen Verabreichung der mRNA-Präparate können eine strenge, Placebo-kontrollierte Studie nicht ersetzen. Dies gilt erst recht bei einer derart mangelhaften Erhebung und Auswertung von Daten über mögliche Impfschäden, wie wir sie derzeit erleben."
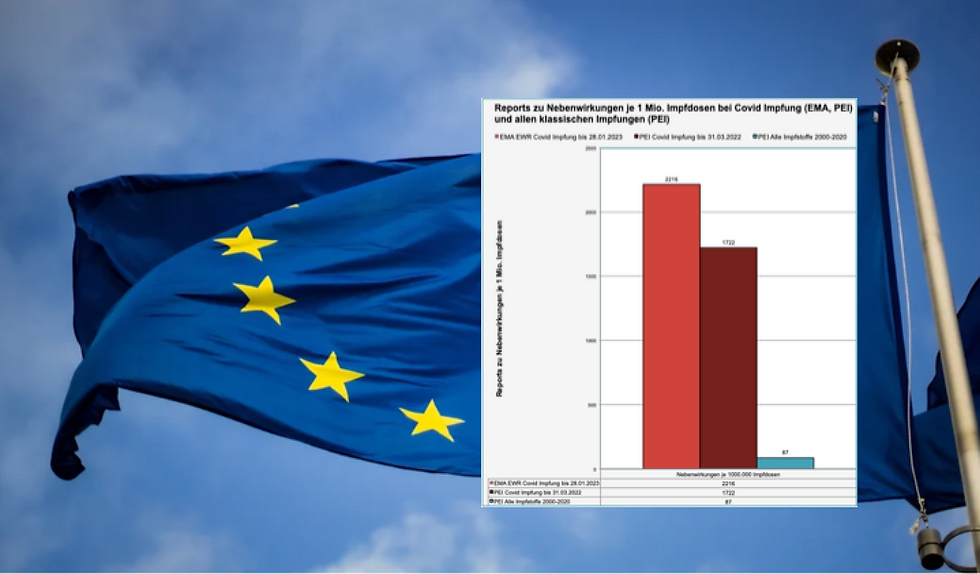
Die EMA EudraVigilanz Datenbank zeigte bereits früh und bis heute dramatische Zahlen von Verdachtsfällen von Impfnebenwirkungen der Covid "Impfstoffe". Wir berichteten.
"Der Lobbyeinfluss bei den Zulassungen führte dazu, dass grundlegende Regeln im Medizinrecht ausgehebelt wurden: Wenn Gesunde geimpft werden, braucht man höhere Sicherheitsstandards, als wenn man schwer kranke Menschen mit Gentherapeutika einem Heilversuch unterzieht."
EMA gab zu, dass Zulassungsstudie nicht fortgeführt werden konnte
Der zuständige CHMP-Ausschuss der EMA gab zu, dass aufgrund des Wegfalls der Kontrollgruppe die Fortführung der Studie sinnlos geworden war. Ein weiterer Erkenntnisgewinn zur Wirksamkeit und Sicherheit des Produktes sei nicht mehr zu erwarten.
Nun hätte die EMA bzw. EU gemäß Art. 20a der Verordnung Nr. 726/2004/EG die Hersteller sanktionieren und die bedingte Zulassung ändern, aussetzen oder widerrufen müssen.

Es geschah aber nichts. Noch fataler: Die Kommission gewährte sogar die reguläre Zulassung, da die Studie nicht weiter fortzuführen sei. Das Juristenteam weist deshalb nachvollziehbar darauf hin, dass diese Verletzung der Verordnungsauflagen damit faktisch belohnt wurde.
Im folgenden soll die Gegendarstellung von Wyler insbesondere zur Rechtmäßigkeit der Zulassung beleuchtet werden.
Gegendarstellung des Molekularbiologen Emanuel Wyler vom Max Delbrück Center der Helmholtz-Gemeinschaft

Wyler geht davon aus, dass es unethisch wäre, Mitglieder der Kontrollgruppe ungeimpft zu lassen.
Menschen wären
"..mitten in einer Pandemie, dem Virus ungeschützt ausgesetzt gewesen, obwohl eine wirksame Impfung zur Verfügung steht. Solche Menschenversuche müssen zu Recht sehr gut begründet werden."
Damit widerspricht er dem Sinn der langjährig bewährten Gesetzgebung für die Arzneimittelzulassung. Nicht umsonst gibt es hierfür ein umfangreiches Regelwerk. Dieses soll gerade durch umfangreiche Auflagen für eine gewissenhafte und umfangreiche Prüfung sicherstellen, dass bei der Allgemeinheit durch nicht ausreichend gesichertes Inverkehrbringung der Arznei-/Impfmittel Schaden entsteht.
Die Aussage geht zudem davon aus, dass Ungeimpfte im Falle einer Infektion einem hohen, nicht verantwortbarem Risiko ausgesetzt würden.
Die Ioannidis Metastudie 01/2023 zur wissenschaftlichen Bestimmung der Gefährlichkeit einer Infektion durch SARS CoV2. Studien und Metastudien zeigen jedoch das sehr niedrige Risiko im Infektionsfalle für Altersgruppen von 0-69 Jahren. Die Sterblichkeitsraten liegen nach dieser Metastudie im Bereich der saisonalen Grippe oder sogar darunter. Wir berichteten.
Ältere oder besonders gefährdete Personengruppen waren jedoch nicht Teilnehmer der Zulassungsstudie.
Die Teilnehmer durften zudem keine nennenswerten Vorerkrankungen aufweisen. Die dänische Erikstrupstudie zeigt für Personen ohne Vorerkrankungen im Alter von 17-72 das extrem niedrige Risiko von nur 0,0102% Sterberisiko im Falle einer Covid Erkrankung. Nur 1 von 10.000 Personen stirbt. Diese sehr niedrige Rate dürfte schon fast dem natürlichen Sterblichkeitsrisiko in diesem Alter entsprechen.
Insofern waren gerade die Studienteilnehmer - allesamt im jungen und mittleren Alter + ohne Vorerkrankungen - nicht so gefährdet, als dass sie nicht weiter in der Kontrollgruppe hätten bleiben können.
Hinzu kommt, dass nicht alle Personen an SARS CoV2 erkranken und folglich die Absolute-Risiko-Reduktion ARR und nicht die Relative-Risiko-Reduktion entscheidend für die Beantwortung solcher Fragen ist. Die ARR lag zum Zeitpunkt der Zulassungsstudie bei nur rund einem Prozent. Das Risiko war folglich dementsprechend niedrig einzuschätzen.
Weiter weiß man seit langem, dass die "Impfung" keinen Fremdschutz bietet. Wir berichteten. Die Ansteckungsgefahr der Teilnehmer kann folglich damit nicht gesenkt werden.
Wyler argumentiert weiter, dass in der bisherigen Zulassungsstudie bis zur Aufgabe der Kontrollgruppe keine Myokarditis Fälle gefunden wurden. Dabei berücksichtigt er jedoch nicht, dass die CDC vor kurzem 770 Sicherheitssignale zu verschiedenen mRNA Impfnebenwirkungen bei der Auswertung der US VAERS Datenbank aufgrund einer rechtlichen Anfrage herausgeben musste.
In 500 Nebenwirkungskategorien waren die Sicherheitssignale dabei stärker als für Myokarditis. Wir berichteten. Es müssten folglich auch diese 500 Nebenwirkungskategorien mit höheren Sicherheitssignalen als bei Myokarditis in die Risikoanalyse mit einbezogen werden.
Selbst wenn Wylers einfache Annahme - nur auf Myokarditis als Impfnebenwirkung käme es an -zutreffend wäre: Die heutigen mRNA Myokarditisraten für jüngere Altersgruppen liegen nach neuen Studien (z.B. Sharff et al. 04/2022) zudem im Bereich 1: 1.800. Nur 1 von 1.800 Personen im Alter von 16-24 Jahren erleidet folglich nach der mRNA Impfung eine Myokarditis. Wir berichteten.
Kein Hinweis auf Interessenkonflikt
Für die Einschätzung der Richtigkeit und Vollständigkeit von Informationen ist es wichtig zu wissen wie neutral und unabhängig von finanziellen Drittinteressen die Informationen gegeben wurden.
Weder Emanuel Wyler noch die Berliner Zeitung weisen dabei auf folgende Interessenkonflikte von Helmholtz hin.
Abhängigkeit der Helmholtz-Gemeinschaft von Öffentlicher Förderung

Emanuel Wyler ist Wissenschaftler am Max Delbrück Center (MDC). Dieses ist Teil der Helmholtz-Gemeinschaft. Der Jahresetat der Helmholtz-Gemeinschaft finanziert sich zu 70 Prozent durch Grundförderung durch Bund und Länder. Die restlichen 30 Prozent kommen aus Drittmittel Fördergeldern. Helmholtz, MDC und Wyler sind somit vollständig abhängig von Fördergeldern des Bundes und der Länder.
Der Etat von 5,8 Milliarden - kein Schreibfehler - in Zahlen 5.800.000.000 Euro ist riesig.
Helmholtz und seine Institute sind darüberhinaus ganz maßgeblich in verschiedene Projekte der SARS-CoV-2-Forschung eingebunden. Das Max Delbrück Center, in dem Emanuel Wyler tätig ist, gehört dazu.

Es wurden folglich direkt vom MDC Helmholtz mit öffentlichen Geldern Forschungen im Bereich der mRNA Themen durchgeführt. Infolgedessen kann man nicht wirklich erwarten, dass Wyler als Vertreter des MDC sich vollständig neutral und unabhängig zu Zulassung spezifischen europäischen oder nationalen Fragestellungen äußern kann.
Die anderen geförderten SARS CoV2 spezifischen Helmholtz Projekte sind hier nachzulesen.
Spendengelder der Bill & Melinda Gates Foundation
Damit nicht genug. Auch Spendengelder der Bill & Melinda Gates Foundation sind geflossen. Die Verflechtungen von Gates und der Gates Foundation mit Impfstoffherstellern, Impfallianz GAVI, CEPI "Coalition for Epidemic Preparedness Innovations“ u.a. sind bekannt.

Im Jahre 2019 erhielt ein Helmholtz Centrum (Helmholtz Zentrum für Infektionsforschung) Spendengelder in Höhe von insgesamt 3.700.000 USD. Auch diese Spendengelder in Millionenhöhe hätten transparenter Weise angegeben werden müssen.
Transparenztest Resümee
Wir haben uns in dieser Analyse nur auf die beanstandeten, nicht erfüllten Zulassungsbedingungen konzentriert. Auf die Fragestellung, wie die mRNA rechtlich und inhaltlich einzuordnen ist (Gentherapie, genbasierte Impfung, modRNA oder sonst etwas) wollten wir hier noch nicht eingehen und in einem gesonderten Beitrag nachholen. Viel entscheidender schien uns jetzt die Frage bezüglich der konkreten Erfüllung der aktuellen Zulassungsbedingungen für mRNA Impfungen.
Die sieben Juristen haben hier Ross und Reiter benannt. Sie geben exakt an, welche Paragraphen bei der Umstellung der bedingten auf die reguläre Zulassung übergangen wurden und auf welcher juristischen Grundlage die EMA/EC hätte reagieren müssen. Hierauf wäre in der Gegendarstellung rechtlich zu antworten gewesen. Dies ist nicht erfolgt.
Liest man die Gegenstellungnahme des Molekularbiologen wird nicht wirklich klar, warum die BZ seinen Argumenten so hohe Bedeutung bemisst. Es ist zwar eine Argumentation und Meinung, die man haben kann. Aber Meinungen gibt es viele. Wirkliche Argumente, die die Rechtsexpertise des 7-köpfigen Juristen-Kollektivs angreifen würden, sind nicht zu erkennen. Das geht auch gar nicht, da eine juristische Bewertung des Zulassungsverfahrens nicht biologisch widerlegt oder eingeschränkt werden kann.
Es wird auch nicht klar, ob Wyler als Privatperson oder als legitimer Vertreter für das MDC oder gar für die Helmholtz-Gemeinschaft diese Gegendarstellung vorträgt.
Man wird den Eindruck nicht los, dass die BZ Druck von "oben" bekommen hat. Anders ist der etwas "unterwürfige" Transparenzhinweis der BZ (Artikel wurde aufgrund von starken Argumenten depubliziert) nicht zu verstehen.
Zuletzt stellt sich die Frage, wie angesichts der enormen finanziellen Abhängigkeit der Helmholtz-Gemeinschaft von öffentlichen Geldern und von B&M Gates Foundation (Beteiligungen bei Moderna, GAVI Impf Alliance, CEPI u.a.) hier eine unabhängige Bewertung durch ein Helmholtz Center in einer Zulassungsfrage für Covid "Impfstoffe" zu erwarten ist. Selbst wenn man eine sachlich fundierte neutrale Auskunft für möglich hält, wäre ein Transparenzhinweis hier zu erwarten gewesen.
Unsere Tt Fragen:
Warum und aufgrund welcher Einwände (von wem) wurde der BZArtikel wirklich zurückgezogen?
Warum geht die Gegendarstellung von Wyler/MDC/Helmholtz nicht auf die juristisch relevanten - und nach Darstellung des Juristen-Kollektivs - nicht erfüllten Zulassungsvorgaben nach Art 14a Abs. 8 der Verordnung Nr. 726/2004/EG und Art. 7 der Kommissionsverordnung Nr. 507/2006/EG ein?
Warum wurden mögliche finanzielle Interessenkonflikte von Wyler/MDC/Helmholtz nicht transparent angegeben?
Ohne Sie geht es nicht!
Unser Ziel ist es uns alle für mehr Transparenz und Evidenz zu sensibilisieren.
Wir Bürger haben ein unabdingbares Recht darauf zu erfahren, was wann wie und aus welchen Gründen - ohne unsere Zustimmung - entschieden wird. Da selten die Informationen vollständig und nachvollziehbar gegeben werden, müssen wir wach bleiben und nachfragen.
Stärken Sie uns mit einem kleinen Beitrag den Rücken, damit wir mit Ihrer Unterstützung dies von den Verantwortlichen einfordern können.
Wir danken Ihnen hierfür herzlich an dieser Stelle, da wir aus Gründen des Datenschutzes auf Spenden nicht antworten dürfen.
Hier klicken
Folgen Sie uns auch auf
https://twitter.com/transparenztest
https://t.me/transparenztest
https://gettr.com/user/transparenztest
Quellen:
https://www.berliner-zeitung.de/politik-gesellschaft/das-zulassungsdesaster-lobbyarbeit-und-rechtsbruch-im-fall-der-mrna-praeparate-li.314750
https://eur-lex.europa.eu/legal-content/DE/TXT/PDF/?uri=uriserv:OJ.C_.2022.457.01.0001.01.DEU
https://www.ema.europa.eu/en/documents/variation-report/comirnaty-h-c-5735-r-0137-epar-assessment-report-renewal_en.pdf
https://www.fda.gov/vaccines-blood-biologics/cellular-gene-therapy-products/what-gene-therapy
https://pharma-kodex.de/3-verordnung-eg-nr-726-2004-des-europaeischen-parlaments-und-des-rates/
https://eur-lex.europa.eu/legal-content/DE/TXT/PDF/?uri=CELEX:32006R0507&from=DE
https://www.helmholtz.de/forschung/im-fokus/coronavirus-sars-cov-2/forschung/
https://transition-news.org/berliner-zeitung-nimmt-kritischen-artikel-zur-verkurzten-covid-impfzulassung
https://reitschuster.de/post/lobbyarbeit-und-rechtsbruch-bei-impf-zulassungen/
https://www.ema.europa.eu/en/about-us/how-we-work/governance-documents/funding

Unsplash: Guillaume Périgois, Spencer Davis


Kommentare